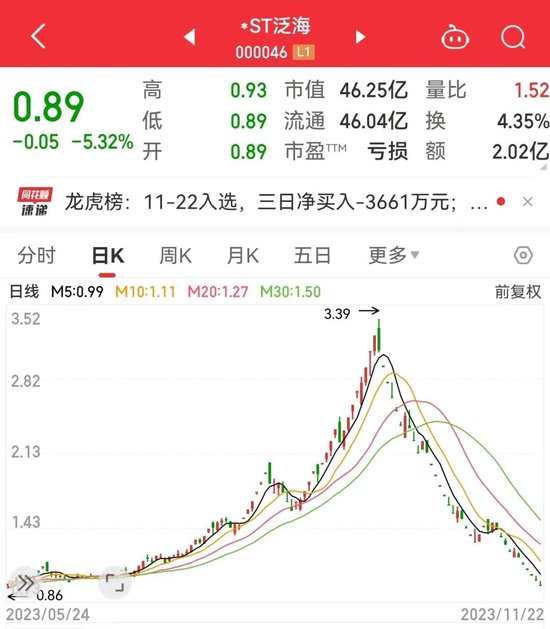
来源:财联社
今年以来,被冠以“减肥神药”之名的司美格鲁肽的关注度依然“高烧不退”,制药商诺和诺德也没有丝毫怠慢,正在尽力推动司美格鲁肽药丸版的审批,据悉该药物最快于明年上市。
据了解,口服版司美格鲁肽早于2019年就通过了美国食品和药品监督管理局(FDA)的审批,但仅用于治疗2型糖尿病,商品名为“Rybelsus”,是全球首个获批的口服GLP-1药物。
其与风靡欧美的减肥针“Wegovy”的药物有效成分同为司美格鲁肽。但与减肥针相比,口服片的优势巨大,其具有超强便利性、更好储存和运输,疗效稳定,禁忌较少,更利于超大规模生产降低成本,势必成为重要爆点。
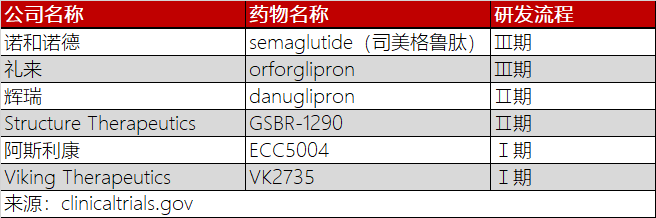
与此同时,礼来、辉瑞、阿斯利康等竞争对手也在争相竞逐口服片领域。两个月前,辉瑞CEO艾伯乐(Albert Bourla)表示,口服片将发挥非常重要的作用,因为并不是每个人都能接受注射治疗。
阿斯利康CEO苏博科(Pascal Soriot)则指出,口服药物能让更多来自低收入国家的人使用到它们。不过,Rybelsus尚未实现这一点,该药物与糖尿病针“诺和泰”(Ozempic)的标价相同,一个月为936美元。
一个月前,诺和诺德在clinicaltrials.gov网站上登记了一项III期研究,旨在评估司美格鲁肽片对比恩格列净或二甲双胍片治疗新诊断2型糖尿病患者的疗效和安全性。若取得积极结果,Rybelsus有望进一步抢占市场份额。

但这种药丸仍然有局限性:患者需要每天空腹服用,然后须再等待半小时才能进食,并且最高剂量的版本报告的胃肠道副作用也明显更多。对此,礼来高管表示,其药物Orforglipron则没有这些限制。
Truist Securities资深生物技术分析师Joon Lee告诉媒体,礼来的药物“看起来是最好的”,虽然距离商业化可能还需要一些时间,但它让礼来具备了在这一领域与诺和诺德展开竞争的潜力。
辉瑞方面则明显落后许多,公司6月份宣布决定放弃第二代的Lotiglipron,全力推进第一代的Danuglipron。辉瑞给出的解释是第二代的Lotiglipron在早期临床中出现的转氨酶升高的安全性信号,而这一问题在第一代的Danuglipron中则没有发现。
除此以外,Viking Therapeutics Inc.和Structure Therapeutics Inc.等生物技术公司也在测试减肥药。BMO资本市场分析师Evan David Seigerman在一份报告中写道,Structure正处于中期人体试验阶段,其令人鼓舞的结果已“绝对领先于”辉瑞。